Abiturwissen Chemie Oberstufe/Proteine/Versuche zur Wirksamkeit von Enzymen/pH- Wert- Untersuchungen: Unterschied zwischen den Versionen
KKeine Bearbeitungszusammenfassung |
KKeine Bearbeitungszusammenfassung Markierung: Quelltext-Bearbeitung 2017 |
||
| Zeile 20: | Zeile 20: | ||
==Beobachtung:== | ==Beobachtung:== | ||
Gefäße mit Essig; Links ohne Speichel - rechts mit | Gefäße mit Essig; Links ohne Speichel - rechts mit | ||
-> Es lässt sich keine (bzw. nur eine minimale) Beobachtung erkennen. | -> Es lässt sich keine (bzw. nur eine minimale) Beobachtung erkennen. | ||
[[Datei:Gefäße mit Essig.png|mini|300x300px|alternativtext=|ohne]] | |||
Gefäße mit basischem Salz; Links mit Speichel - rechts ohne | Gefäße mit basischem Salz; Links mit Speichel - rechts ohne | ||
-> Es lässt sich eine leichte Entfärbung von beiden Lösungen erkennen; bei der Lösung mit Speichel (links) tritt eine etwas stärkere Einfärbung auf. | -> Es lässt sich eine leichte Entfärbung von beiden Lösungen erkennen; bei der Lösung mit Speichel (links) tritt eine etwas stärkere Einfärbung auf. | ||
[[Datei:Gefäße mit basischem Salz.png|mini|alternativtext=|ohne|299.8x299.8px]] | |||
==Deutung== | ==Deutung== | ||
Aktuelle Version vom 11. April 2021, 17:29 Uhr
pH- Wert– Untersuchungen
Benötigte Materialien und Chemikalien:
- 4 Gefäße
- Stärke
- Wasser
- Iodlösung (Betaisodona- Lösung)
- Speichel
- Essig
- Basisches (Bade)salz o.ä.
Versuchsdurchführung:
Als erstes wird eine Stärkelösung hergestellt, die anschließend langsam mit der Iodlösung versetzt wird bis eine blaue (violette) Färbung eintritt. Diese Verfärbung sollte auch nach dem Schütteln/ Rühren erhalten bleiben. (-> wie beim Vorversuch)
Die Lösung wird anschließend auf 4 Gefäße aufgeteilt.
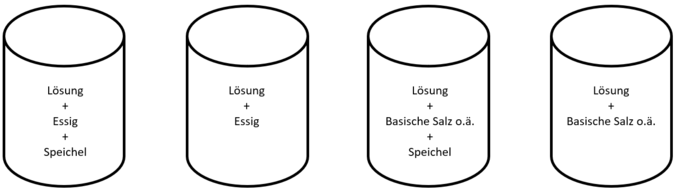
In die Gefäße gibt man, wie im Bild gezeigt, zur Lösung jeweils entsprechend Essig oder basisches Salz o.ä. und ergänzt die Mischung jeweils einmal mit Speichel. Dann rührt man das Ganze um.
Beobachtung:
Gefäße mit Essig; Links ohne Speichel - rechts mit
-> Es lässt sich keine (bzw. nur eine minimale) Beobachtung erkennen.
Gefäße mit basischem Salz; Links mit Speichel - rechts ohne
-> Es lässt sich eine leichte Entfärbung von beiden Lösungen erkennen; bei der Lösung mit Speichel (links) tritt eine etwas stärkere Einfärbung auf.
Deutung
Im Vorversuch wurde deutlich, dass Amylase Stärke abbaut (dieses erkennt man durch die Entfärbung der Lösung). Durch die minimale Entfärbung des jetzigen PH-Wert-Versuches stellen wir fest, dass Amylase Stärke im sauren oder basischen Milieu nicht abbaut. Dadurch wird deutlich, dass Amylase nur innerhalb eines bestimmten pH-Bereichs arbeitsfähig ist.
Diese Feststellung hängt mit den Eigenschaften des Enzyms (Proteins) zusammen. Die biologische Funktion von Enzymen (Proteinen) hängt mit der räumlichen Struktur zusammen. Diese wird durch Säuren bzw. Laugen angegriffen oder zerstört (-> Denaturierung). Das geschieht durch eine Veränderung der Ladungsverhältnisse im Molekül, so dass die Ionenbindungen zwischen den Carboxyl- und Aminogruppen und den Wasserstoffbrücken zerstört werden. Dadurch verändert sich die räumliche Struktur des Enzyms und es verliert seine räumliche Struktur und damit auch seine Funktion.