Abiturwissen Chemie Oberstufe/Proteine/Peptide/Peptidbindung: Unterschied zwischen den Versionen
Keine Bearbeitungszusammenfassung |
(Grafiken korrigiert) |
||
| Zeile 7: | Zeile 7: | ||
<big>Reaktionsmechanismus auf Molekularebene:</big> | <big>Reaktionsmechanismus auf Molekularebene:</big> | ||
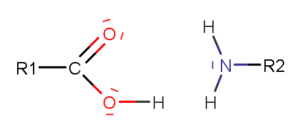
[[Datei: | [[Datei:Peptidbindung1.png|alternativtext=|links|mini|Eine Carbonsäure und eine Aminogruppe]] | ||
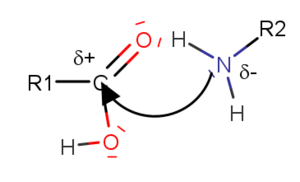
[[Datei: | [[Datei:Peptidbindung2.png|alternativtext=|links|mini|Anlagern der Aminogruppe an das C-Atom der Carboxylgruppe]] | ||
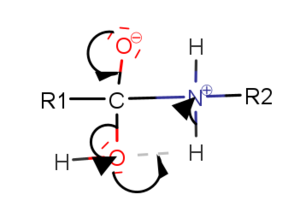
[[Datei: | [[Datei:Peptidbindung3.png|alternativtext=|links|mini|Stabilisieren des entstehenden Moleküls durch Abspalten von Wasser]] | ||
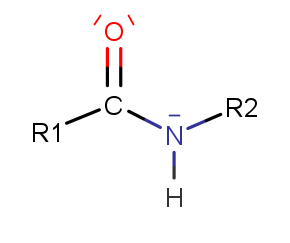
[[Datei: | [[Datei:Peptidbindung4.png|alternativtext=|links|mini|Fertiges Dipeptid inklusive Peptidbindung liegt vor]] | ||
Version vom 22. März 2022, 20:02 Uhr
Die Peptidbindung verbindet einzelne Aminosäuren miteinander und ist damit Voraussetzung zur Bildung von Peptidketten respektive Proteinen. Peptidbindungen enstehen bei einer Kondensationsreaktion unter Abspaltung von Wasser, wobei eine so genannte Peptidgruppe (-CO-NH-) ensteht.
Bei den, an der Bildung beteiligten, funktionellen Gruppen handelt es sich zum einen um die Carboxygruppe einer Aminosäure und zum anderen um eine Aminogruppe einer anderen Aminosäure. Bei der Reaktion kommt es folgend zur Abspaltung der Hydroxygruppe von der Carboxygruppe und zur Abspaltung eines Wasserstoffprotons von der Aminogruppe. Wasserstoffproton und Hydroxygruppe bilden anschließend das abgespaltene, kondensationstypische Wassermolekül.
Reaktionsmechanismus auf Molekularebene: