Abiturwissen Chemie Oberstufe/Organische Chemie/Carbonylgruppe
1. Allgemeines
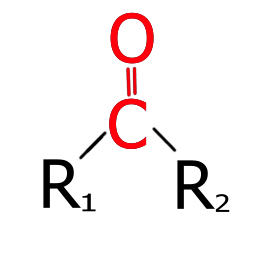
Die Carbonylgruppe, kurz CO-Gruppe, ist eine funktionelle Gruppe und ist Bestandteil vieler organischen-chemischen Verbindungen.
Die Carbonylgruppe ist gekennzeichnet, dass sie aus einem Kohlenstoff- und einem Sauerstoffatom besteht, diese ist über eine Doppelbindung verbunden. (Siehe Bild)
Wenn ein Molekül eine Carbonylgruppe besitzt, so wird die Verbindung auch als Carbonylverbindung bezeichnet.
Die Carbonylgruppe ist Bestandteil dieser organischen-chemischen Verbindungen:
- Carbonsäuren (-COOH)
- Carbonsäureamiden (-CO-NH-)
- Imide (-CO-NH-CO-)
- Carbonsäureanhydriden (-CO-O-CO-)
- Carbonsäureestern (-CO-O-R)
- Carbonsäurehalogeniden (-CO-X (X = F, Cl, Br, I, At))
- Aldehyden/Alkanalen (-CHO)
- Ketonen/Alkanonen (-CO-)
- Urethane (-NH-CO-O-)
- Carbonsäureazide (-CO-N3)
2. Hintergrund
Carbonylgruppen sind eine charakteristische funktionelle Gruppe der Aldehyde und Ketone:
- Aldehydgruppen
- Ketogruppen
Diese enthalten in ihrer Formel eine Carbonylgruppe.
3. Eigenschaften
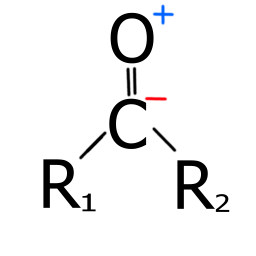
Aufgrund der Polarität (Das Sauerstoffatom besitzt eine negative, das Kohlenstoffatom besitzt dagegen eine positive Partialladung) ist die Carbonylgruppe der Hauptgrund für das physikalische und chemische Verhalten der enthaltenden Moleküle.
Die Polarität führt auch dazu, dass die Carbonylverbindung einen höheren Schmelz-/Siedepunkt als Carbonylfreieverbindungen haben.
Die hohe Reaktivität der Carbonylgruppe ist wegen der polaren Doppelbindung zwischen dem Sauerstoff und dem Kohlenstoff. Wegen dieser Eigenschaft, kann die Bindung von Nukleophilen besser angegriffen werden.
Kurzkettige Aldehyde und Ketone sind gut wasserlöslich, dies liegt daran, dass das Sauerstoffatom der Carbonylgruppe Wasserstoff-Brücken mit dem Wasser bilden kann. Untereinander können diese keine Wasserstoff-Brücken bilden. Aus diesem Grund, liegt der Siedepunkt tiefer, als der bei den Alkoholen.
4. Vorkommen (Beispiele)
- Aceton (Ein Lösungsmittel und im Nagellackentferner enthalten)
- Formaldehyd (Ein Konservierungsmittel für medizinische Präparate)
- Essigsäure (Enthalten in Speiseessig)
- Phosgen (Ein hoch-reaktives Produkt der chemischen Chemie)
- Kohlensäure (In gelöster Form von Kohlendioxid im Sprudelwasser)
- Glycin (Ein Baustein von Proteinen)
- Polycarbonate (Ein Material, aus dem z.B. CD's bestehen)
- Flavone (Blütenfarbstoffe)
GtCHP21 (Diskussion) 16:40, 7. Jan. 2021 (CET)