Abiturwissen Chemie Oberstufe/Fette/Verseifung: Unterschied zwischen den Versionen
KKeine Bearbeitungszusammenfassung |
KKeine Bearbeitungszusammenfassung |
||
| Zeile 19: | Zeile 19: | ||
Im letzten Schritt stabilisiert sich das Alkoholat-Ion. Dieses geschieht durch Aufnahme von Protonen der Carboxylgruppe. (3 und 4) | Im letzten Schritt stabilisiert sich das Alkoholat-Ion. Dieses geschieht durch Aufnahme von Protonen der Carboxylgruppe. (3 und 4) | ||
Aktuelle Version vom 24. November 2020, 18:43 Uhr
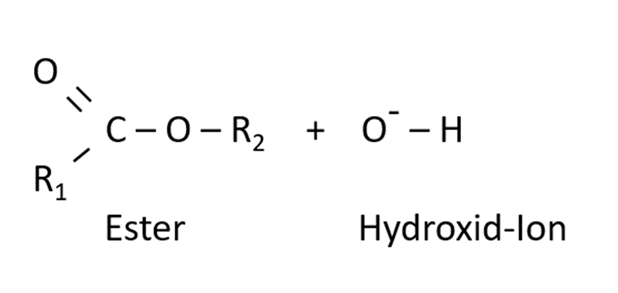
Unter Verseifung wird die Hydrolyse eines Esters durch ein Hydroxid-Ion beschrieben.
Die Edukte der Reaktion sind Ester und Hydroxid-Ionen
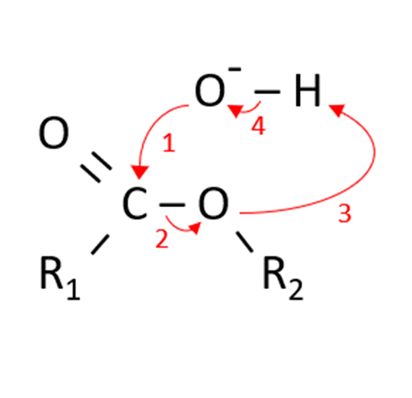
Die Reaktion kann in drei Schritte unterteilt werde, die aufgrund einer Verschiebung der Protonen nahezu gleichzeitig passieren.
1. Schritt: Nukleophiler Angriff des Hydroxid-Ions
Im ersten Schritt greift das negativ geladene Hydroxid-Ion das partiell positiv geladene C-Atom der Estergruppe nucleophil an. (1)
2. Schritt: Abspaltung des Alkoholat-Ions und Bildung der Carbonsäure
Im zweiten Schritt verschiebet sich das Elektronenpaar innerhalb der C-O-Einfachbindung (2). Dadurch wird das Alkoholat-Ion (O- – R2) abgespalten. Es bilden sich „kurzzeitig“ ein Carbonsäuremolekül und ein Alkoholat-Ion. In diesem Schritt handelt es sich um eine Eliminierungsreaktion.
3. Schritt: Protonenübergang vom Carbonsäuremolekül auf das Alkoholat-Ion (irreversibler Schritt der Verseifung)
Im letzten Schritt stabilisiert sich das Alkoholat-Ion. Dieses geschieht durch Aufnahme von Protonen der Carboxylgruppe. (3 und 4)
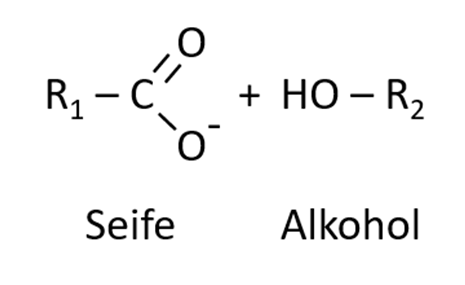
Als Produkte entstehen ein Säure-Anion/ Seifenmolekül und ein Alkoholmolekül.